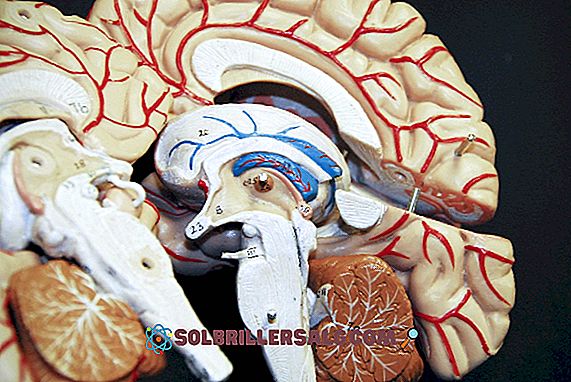
Hiposulfato rūgštis: formulės, charakteristikos ir naudojimo būdai
Hiposulfato rūgštis arba ditiono rūgštis yra nežinoma, grynoje formoje nestabili, neturi nepriklausomo egzistavimo ir nėra aptikta ir vandeniniame tirpale.
Teoriškai tai būtų palyginti silpna rūgštis, panaši į sieros rūgštį H2SO3. Žinomos tik jos druskos, stabilios ir galingos redukuojančios medžiagos. Ditiono rūgšties natrio druska yra natrio ditionitas.

- Formulės
| ditiono rūgšties | ditionitų anijonas | natrio ditionitas | |
| Formulės | H2S2O4 | S2O42- | Na2S2O4 |
- CAS : 20196-46-7 Hyposulfuric acid (arba ditiono rūgštis)
- CAS : 14844-07-6 Hyposulfuric rūgštis (arba ditionis, jonas)
- CAS : 7775-14-6 natrio ditionitas (ditiono rūgšties natrio druska)
2D struktūra


3D struktūra



Savybės
Fizinės ir cheminės savybės
| ditiono rūgšties | ditionitų anijonas | natrio ditionitas | |
| Išvaizda: | , | , | Balti arba pilkšvi kristaliniai milteliai |
| , | , | Šviesūs citrinų spalvos dribsniai | |
| Kvapas: | , | , | Silpnas sieros kvapas |
| Molekulinė masė: | 130, 132 g / mol | 128, 116 g / mol | 174, 096 g / mol |
| Virimo temperatūra: | , | , | Jis suskaido |
| Lydymosi temperatūra: | , | , | 52 ° C |
| Tankis: | , | , | 2, 38 g / cm3 (bevandenis) |
| Tirpumas vandenyje | , | , | 18, 2 g / 100 ml (bevandenis, 20 ° C) |
Hyposulfuric rūgštis yra sieros okso rūgštis, kurios cheminė formulė yra H2S2O4.
Sieros okso rūgštys yra cheminiai junginiai, kuriuose yra sieros, deguonies ir vandenilio. Tačiau kai kurie iš jų yra žinomi tik dėl jų druskų (pvz., Hidroculfato rūgšties, ditiono rūgšties, disulfido rūgšties ir sieros rūgšties).
Tarp apibūdintų okso rūgščių struktūrinių savybių turime:
- Tetrahedinė siera, suderinta su deguonimi
- Deguonies atomai tiltu ir terminalu
- Terminų butxo grupės
- S = S terminalai
- (-S-) n grandinės
Sieros rūgštis yra labiausiai žinoma sieros oksido rūgštis ir svarbiausia pramoninė.
Ditionitų anijonas ([S2O4] 2-) yra sieros oksoionas (jonas, turintis bendrą formulę AXOY z-), formaliai išvestas iš ditiono rūgšties.
Ditionitų jonai hidrolizuojasi tiek rūgšties, tiek šarminės prie tiosulfato ir bisulfito bei sulfito ir sulfido.

Ditiono rūgšties natrio druska yra natrio ditionitas (taip pat žinomas kaip natrio hidrosulfitas).
Natrio ditionitas yra baltos spalvos iki šviesiai geltonos spalvos milteliai, kurių kvapas panašus į sieros dioksidą.
Jis spontaniškai sušildo susilietus su oru ir drėgme. Ši šiluma gali pakakti aplinkinių degių medžiagų užsidegimui.
Ilgai veikiant gaisrui ar intensyviai karščiui, šios medžiagos talpyklos gali smarkiai sulūžti.
Jis naudojamas kaip reduktorius ir kaip balinimo priemonė. Jis naudojamas ir balinantis popieriaus plaušieną bei dažymą. Jis taip pat naudojamas nitro grupei redukuoti į amino grupę organinėse reakcijose.
Nors daugeliu atvejų jis yra stabilus, jis suyra karštame vandenyje ir rūgštiniuose tirpaluose.
Jis gali būti gaunamas iš natrio bisulfito pagal šią reakciją:
2 NaHSO3 + Zn → Na2S2O4 + Zn (OH) ²
Oro ir vandens reakcijos
Natrio ditionitas yra degi kieta medžiaga, kuri lėtai suyra, kai liečiasi su vandeniu ar vandens garais, susidaro tiosulfatai ir bisulfitai.
Ši reakcija sukuria šilumą, kuris gali dar labiau paspartinti reakciją arba sukelti aplinkinių medžiagų degimą. Jei mišinys yra uždarytas, skilimo reakcija gali sukelti konteinerio slėgį, kuris gali būti smarkiai pažeistas. Kai jis lieka ore, jis oksiduojasi lėtai ir sukelia toksiškas sieros dioksido dujas.
Gaisro pavojus
Natrio ditionitas yra degi ir degi medžiaga. Jis gali užsidegti, esant sąlyčiui su drėgnu oru. Jis gali greitai sudegti, kai atsiranda efektas. Jis gali energingai arba sprogiai reaguoti su vandeniu.
Šildant ar gaisro metu jis gali sprogti. Po to, kai gaisras išnyksta, jis gali atkurti. Nuotėkis gali sukelti gaisro ar sprogimo pavojų. Šildant konteineriai gali sprogti.
Pavojus sveikatai
Patekus ant ugnies, natrio ditionitas sukels dirginančias, ėsdinančias ir (arba) toksiškas dujas. Skilimo produktų įkvėpimas gali sukelti rimtą sužalojimą ar mirtį. Patekimas į medžiagą gali sukelti sunkius odos ir akių nudegimus. Nuotėkis iš gaisro gali sukelti taršą.
Naudojimas
Ditionito joną, dažnai kartu su kompleksiniu agentu (pvz., Citrinos rūgštimi), naudojamas geležies (III) oksihidroksido redukavimui į tirpius geležies (II) junginius ir amorfinių geležies turinčių mineralinių fazių pašalinimą (III) dirvožemio analizėje (selektyvi ekstrakcija).
Ditionitas leidžia padidinti geležies tirpumą. Dėl ditionito jonų stipraus afiniteto dvivalentiams ir trivalentiems metaliniams katijonams, jis naudojamas kaip chelatinis agentas.
Ditionito skilimas mažina sieros rūšis, kurios gali būti labai agresyvios plieno ir nerūdijančio plieno korozijai.
Tarp natrio ditionito taikymų mes turime:
Pramonėje
Šis junginys yra vandenyje tirpi druska ir gali būti naudojamas kaip redukcinis agentas vandeniniuose tirpaluose. Jis naudojamas kaip pramoninis dažymo procesas, daugiausia susijęs su sieros dažais ir tepalo dažais, kuriuose vandenyje netirpūs dažai gali būti redukuojami į vandenyje tirpią šarminių metalų druską (pavyzdžiui, indigo dažus). ).
Sumažinant natrio ditionito savybes, taip pat pašalinamas perteklius, likęs oksidas ir nepageidaujami pigmentai, taip pagerinant bendrą spalvų kokybę.
Natrio ditionitas taip pat gali būti naudojamas vandens valymui, dujų valymui, valymui ir ekstrahavimui. Jis taip pat gali būti naudojamas pramoniniuose procesuose kaip sulfonavimo agentas arba natrio jonų šaltinis.
Be tekstilės pramonės, šis junginys naudojamas pramonėje, susijusioje su oda, maistu, polimerais, fotografija ir daugeliu kitų. Jis taip pat naudojamas kaip spalvos mažinimo agentas organinėse reakcijose.
Biologijos moksluose
Natrio ditionitas dažnai naudojamas fiziologiniuose eksperimentuose, siekiant sumažinti tirpalų redokso potencialą.
Geologijos moksluose
Natrio ditionitas dažnai naudojamas dirvožemio chemijos eksperimentuose, siekiant nustatyti geležies kiekį, kuris nėra įtrauktas į pirminius silikatinius mineralus.
Saugumas ir rizika
Pasauliniu mastu suderintos cheminių medžiagų klasifikavimo ir ženklinimo sistemos pavojingumo pareiškimai
Pasauliniu mastu suderinta cheminių medžiagų klasifikavimo ir ženklinimo sistema (SGA) yra tarptautiniu mastu suderinta sistema, sukurta Jungtinių Tautų ir sukurta siekiant pakeisti įvairius klasifikavimo ir ženklinimo standartus, naudojamus įvairiose šalyse, naudojant nuoseklius pasaulinius kriterijus.
Pavojaus klasės (ir jų atitinkamas GHS skyrius), klasifikavimo ir ženklinimo standartai ir rekomendacijos natrio ditionitui yra šios (Europos cheminių medžiagų agentūra, 2017, Jungtinių Tautų Organizacija, 2015, PubChem, 2017):